药物临床试验是个什么鬼?
发布日期:2018-09-19 来源:深圳市宝安区妇幼保健院“神农尝百草”是一个流传至今的美丽传说,也是最早、最原始的药物临床试验。我们的神农简单粗暴的直接把发现的草药植物塞进自己口里不管自己死活的精神让我们感动,但是科技发展到今天,药物临床试验还是如此简单粗暴吗?

答案肯定是 No
要回答这个问题,我们先要搞清楚我们所吃的药物从何而来?

一个药物到我们手上之前已经经历了药物研发、临床前试验、临床试验及上市后在评价阶段,所以我们今天吃的药物绝不是这么简单的就可以到我们的手上,反而经历过这么一个漫长而复杂的过程之后,只剩下不到1%的成品药物可以到我们手上。
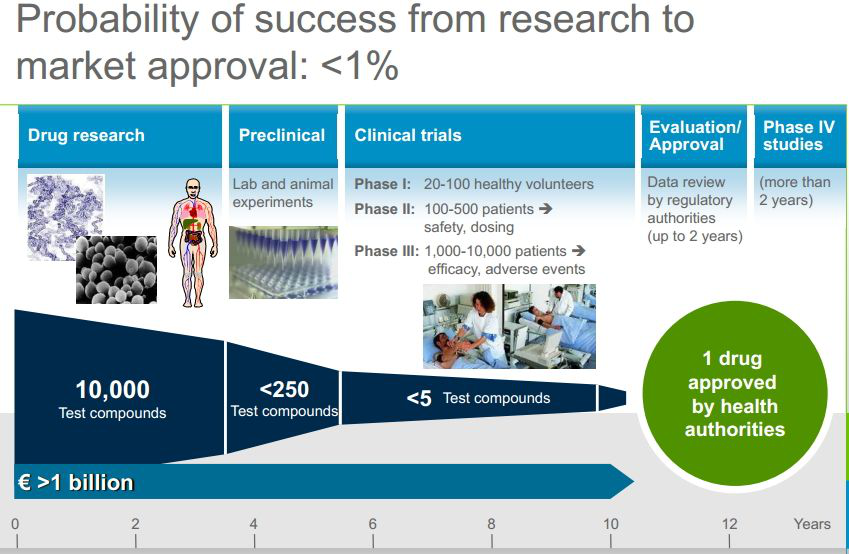
新药研发过程主要包括苗头分子的发现、细胞活性评价、非临床药理毒理研究、临床试验和上市后的安全性监督。其中临床试验耗资/耗时基本占整个新药开发的60%~80%,可谓是新药开发最耗钱耗时的阶段。每一种新药在投放市场前,都必须经过临床试验,在此过程中“试药人”作为一个低调的群体,为新药的诞生做出了巨大贡献。
对于多数人而言,药物临床试验似乎是个陌生而遥远的事物。出于对安全的担心会对它“敬而远之”,不想做所谓的“小白鼠”,很多人甚至将参加药物临床试验当做“不治之症最后的选择”,然而对于药物临床试验的真正定义及过程是怎样的并不为人所熟知。
一、药物临床试验的定义
药物临床试验是指任何在人体(病人或健康志愿者)进行的药物的系统性研究,以证实或发现试验药物的临床、药理和/或其他药效学方面的作用、不良反应和/或吸收、分布、代谢及排泄,从而确定试验药物的安全性和有效性。
如果早期实验室研究(如细胞培养和动物实验),显示药物有应用前景,企业就可以向FDA提交新药研究申请,获批后才可以进行人体试验,这时候才是真正进入临床研究阶段,药物的早期研发一般需要2~6.5年时间。
二、药物临床试验所遵循的基本原则
药物临床试验是多种专业技术人员共同合作而进行的。这些专业人员不仅应包括医学、药学、药理学、生物学、生物统计学等,还应包括非医学专业的但富有经验的文档管理人员。这些人员还要熟知药物临床试验的研究过程和有关的法规、标准和原则。由于药物临床研究的方法、手段、目的的特殊性,例如,需要人类受试者的参与、药物临床试验的资料和结果需要经过药品监督管理部门的审批等,药物临床研究与一般的科学研究不同,需要满足更多的条条框框,遵循更多的原则。概括地讲,所有药物临床试验必须遵循下列三项基本原则:
·伦理道德原则;
·科学性原则;
·GCP与现行法律法规。
三、药物临床试验的分期
FDA将临床研究分为三期,这三期临床研究通常按期依次实施,但也可以有重叠;另外针对新药批准上市后的临床研究,FDA定义其为IV期临床试验。ICH(国际药品技术要求协调组织)根据临床研究的目的将临床试验同样分为IV期。
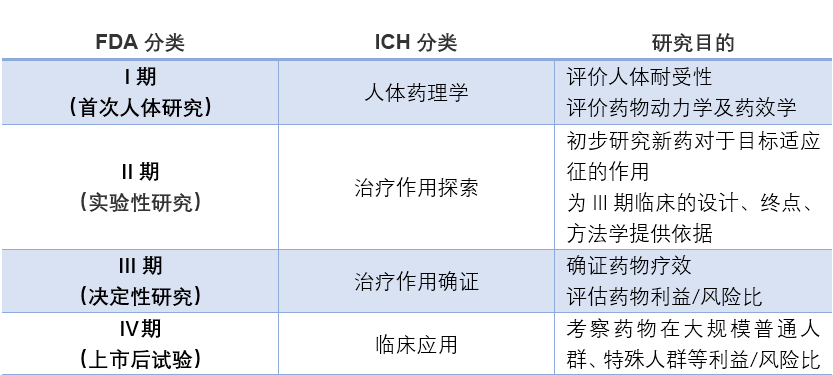
I期临床试验:一般从单剂量开始, 在严格控制的条件下,给少量试验药物于少数(10?100例)经过谨慎选择和筛选出的健康志愿者(对肿瘤药物而言通常为肿瘤病人),然后仔细监测药物的血液浓度、排泄性质和任何有益反应或不良作用,以评价药物在人体内的药代动力学和耐受性。通常要求志愿者在研究期间住院,每天对其进行24h的密切监护。随着对新药的安全性了解的增加,给药的剂量可逐渐提高,并可以多剂量给药。
II期临床试验:重点在于研究药物的安全性和疗效, 应用安慰剂或已上市药物作为对照药物对新药的疗效进行评价,在此过程中对疾病的发生发展过程对药物疗效的影响进行研究;确定Ⅲ期临床试验的给药剂量和方案;获得更多的药物安全性方面的资料。
Ⅲ期临床试验:进一步验证药物对目标适应症患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请的审查提供充分的依据。
如果Ⅲ期临床试验表明药物安全有效,企业就可以向FDA提交新药申请(要提交动物试验和人体试验的数据、预期药物生产流程、处方信息和产品说明书等材料),FDA将对所有信息进行评估,并决定该药物的安全性与有效性是否达到上市要求。得到FDA批准后,药物才可以上市。FDA的评估过程一般需要0.5~1年时间。平均来说,在实验室研究的4000个药物中只有大约5个能进行人体试验,而这5个之中又只有1个能最终获得批准上市。
IV期临床试验:一种新药在获准上市后,企业仍然需要进行进一步的研究,在广泛使用条件下考察其疗效和不良反应。一些罕见的重要不良反应只能在用于大量人群后,即上市后才可能发现。长期用药可能出现的问题,也只能在这个阶段来发现。

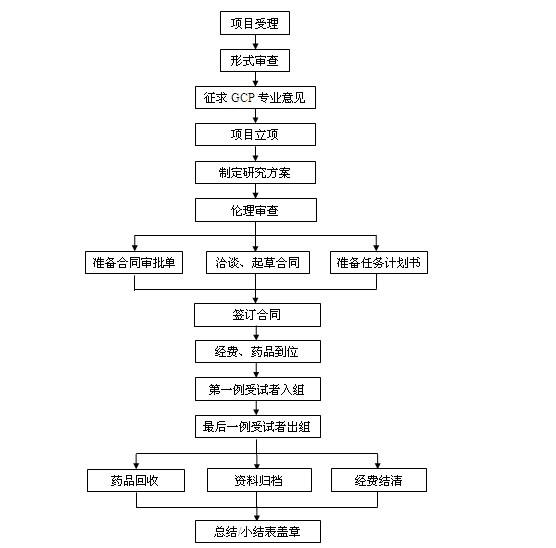
每一项药物临床试验的开展都必须由国家药品监督管理局审查批准。并按照以下的流程完成该项新药试验。而可以进行药物临床试验的机构就称为药物临床试验机构,目前全国有627家药物临床试验机构,且其中有91家可开展儿科药物临床试验,而广东省有56家临床试验机构包括10家具有儿科药物临床试验的机构。
审稿专家:深圳市宝安区妇幼保健院 郭惠娟

相关文章
标签 药物临床试验
- 解读关键字:药物临床试验2021-05-02
- 药物临床试验知多少?2021-04-07
- 什么是药物临床试验?2017-12-09









